本文系基于公開資料撰寫,僅作為信息交流之用,不構(gòu)成任何投資建議。
2025年,中國抗流感用藥市場迎來“國產(chǎn)元年”。
青峰醫(yī)藥的瑪舒拉沙韋片、眾生藥業(yè)的昂拉地韋片、濟(jì)川藥業(yè)的瑪硒洛沙韋片相繼獲批,成為首批上市的國產(chǎn)創(chuàng)新抗流感藥。同時,健康元的瑪帕西沙韋、先聲藥業(yè)的瑪氘諾沙韋亦已提交新藥上市申請,距離正式獲批僅一步之遙。
這些藥品多為RNA聚合酶抑制劑,對標(biāo)藥物為羅氏旗下被稱作“流感神藥”的瑪巴洛沙韋片(商品名:速福達(dá)),作用機(jī)制接近。
國內(nèi)藥企紛紛布局抗流感藥物賽道,其背后既是基于對該市場擴(kuò)容潛力的長期看好(預(yù)計由2023年107.4億元增至2028年269億元的),更與瑪巴洛沙韋的銷售奇跡直接相關(guān)(2023年突破5億元,同比漲幅達(dá)758%)。
然而,市場狂歡的表象之下,違規(guī)營銷暗流涌動、用藥風(fēng)險被刻意淡化、臨床數(shù)據(jù)短板亟待補(bǔ)齊等問題逐步顯現(xiàn)。圍繞“流感神藥”掀起的市場熱潮,究竟是中國制藥升級的里程碑,還是藥物濫用與網(wǎng)紅營銷合謀的危險狂歡?
01
突破與瓶頸
靠著“全病程只需服用一次”的優(yōu)勢,瑪巴洛沙韋重構(gòu)了抗流感藥物的市場規(guī)則。
但需明確的是,瑪巴洛沙韋的耐藥性問題早已在海外顯現(xiàn),且最早出現(xiàn)于其2018年2月首次獲批的日本市場。
《問藥師》創(chuàng)始人冀連梅近期撰文指出,日本在2018/2019流感季大規(guī)模使用瑪巴洛沙韋后,便出現(xiàn)了耐藥病毒,不僅導(dǎo)致部分患者流感復(fù)發(fā)或病程延長,兒童的耐藥比例亦顯著高于成人;美國藥品說明書亦在“警告和注意事項(xiàng)”欄目中明確,因5歲以下兒童易產(chǎn)生耐藥性,該藥物不適用于這一人群。
為了實(shí)現(xiàn)差異化競爭,國產(chǎn)藥企將“降低耐藥率”視為核心突破方向。
青峰醫(yī)藥的瑪舒拉沙韋片與瑪巴洛沙韋同為PA亞基靶點(diǎn),其Ⅲ期臨床研究數(shù)據(jù)更具優(yōu)勢。該藥物對甲型流感H1N1和H3N2亞型病毒的耐藥突變率僅為0.7%和0.9%,乙型流感患者中未檢測到耐藥突變,耐藥性表現(xiàn)突出。
而眾生藥業(yè)的昂拉地韋片則另辟蹊徑,瞄準(zhǔn)PB2靶點(diǎn)展開研發(fā)。在Ⅱ期和Ⅲ期試驗(yàn)中,瑪巴洛沙韋接受者分別有2.2%和9.7%出現(xiàn)了藥物敏感性降低情況,而昂拉地韋接受者的這一比例僅為0和1.6%,展現(xiàn)出更優(yōu)的耐藥性表現(xiàn)。
不過,新藥并非“完美解”,不良反應(yīng)仍需長期觀察。
從歷史發(fā)展維度來看,抗流感藥物的適應(yīng)癥審批進(jìn)程有其規(guī)律,既適配流感病毒的變異迭代,也貼合臨床研究的持續(xù)深化,還與臨床用藥需求的動態(tài)變化相契合。
以瑪巴洛沙韋為例,其在國內(nèi)獲批上市的時間僅四年,但該藥經(jīng)不良反應(yīng)監(jiān)測發(fā)現(xiàn),存在過敏性休克、血管性水腫、蕁麻疹等嚴(yán)重過敏反應(yīng);而瑪舒拉沙韋片、瑪硒洛沙韋片、昂拉地韋片三款國產(chǎn)新藥于2025年方才完成獲批,尚未在大規(guī)模、多樣化的人群中完成長期驗(yàn)證,相關(guān)不良反應(yīng)的臨床反饋數(shù)據(jù)亦十分有限。
其次,新一代抗流感新藥在適應(yīng)癥的人群年齡界定上,普遍呈現(xiàn)出“收窄化”的顯著特征,這也成為制約其臨床推廣應(yīng)用的核心因素。經(jīng)統(tǒng)計,瑪巴洛沙韋片、瑪舒拉沙韋片的適用人群分別限定為5歲及以上、12歲及以上,瑪硒洛沙韋片與昂拉地韋片則僅適用于18歲及以上成人。
這類適應(yīng)癥限制,把5歲以下兒童、12-18歲青少年等流感高發(fā)群體,排除在多款新型抗流感藥物的適用范圍之外。臨床醫(yī)師為這類人群制定用藥方案時,難以借助新藥臨床數(shù)據(jù)形成科學(xué)指導(dǎo),新型抗流感藥物的實(shí)際臨床應(yīng)用場景也因此被大幅壓縮。
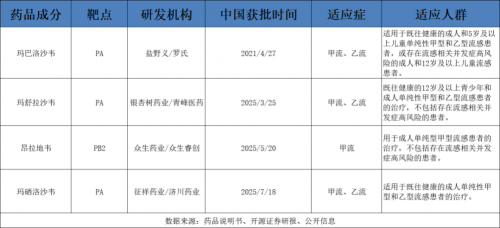
圖:流感藥物的局限性,來源:開源證券
若超適應(yīng)癥使用此類新型抗流感藥物,將潛藏極大的臨床風(fēng)險。
最為常見的案例便是瑪巴洛沙韋片的不當(dāng)使用。其藥品說明書明確標(biāo)注不適用于5歲以下兒童,但仍有家長在社交媒體分享給低齡兒童服用該藥物的經(jīng)歷。

圖:瑪巴洛沙韋片用藥誤區(qū),來源:小紅書截圖
在孕婦群體中,亦有患者在社交平臺表示,感染流感后服用了瑪巴洛沙韋片,因而對胎兒安全產(chǎn)生極大擔(dān)憂。事實(shí)上,瑪巴洛沙韋片說明書顯示,該藥物尚未在妊娠女性中開展充分且對照良好的臨床研究,其潛在風(fēng)險尚未明確。此外,動物實(shí)驗(yàn)結(jié)果表明,向妊娠家兔投喂高劑量瑪巴洛沙韋片,會引發(fā)母體毒性,并導(dǎo)致家兔流產(chǎn)。
盡管國產(chǎn)流感新藥針對瑪巴洛沙韋痛點(diǎn)實(shí)現(xiàn)破局,但卻仍存在諸多現(xiàn)實(shí)瓶頸,難稱版本答案。
02
“種草”亂象
藥物應(yīng)該進(jìn)行營銷推廣嗎?這是傳媒行業(yè)長期爭論的議題之一。事實(shí)上,瑪巴洛沙韋等流感神藥的走紅,離不開社交媒體的“流量加持”,但此類營銷行為或已觸碰法律紅線。
在微博、小紅書、抖音等社交平臺,大量博主以“個人經(jīng)驗(yàn)分享”為名,變相推廣瑪巴洛沙韋片、瑪舒拉沙韋片等流感處方藥。部分博主通過“這款流感特效藥效果顯著”“甲流特效藥,親測有效”等夸張表述,夸大藥物療效。
但鮮少有博主提及,瑪巴洛沙韋不可與乳制品、鈣強(qiáng)化飲料、含高價陽離子的瀉藥、抗酸藥或口服補(bǔ)充劑(如鈣、鐵、鎂、硒或鋅)同時服用。
這些看似真實(shí)的分享,很多可能暗藏商業(yè)利益。中國社會科學(xué)院大學(xué)互聯(lián)網(wǎng)法治研究中心主任劉曉春表示,純粹的個人經(jīng)驗(yàn)分享并不違法,要防范的,是假借個人分享為名進(jìn)行商業(yè)推銷。“特別是涉及藥品這種高風(fēng)險的產(chǎn)品,說得不夠準(zhǔn)確的話,可能會導(dǎo)致很嚴(yán)重的后果。因此,藥品廣告是受到嚴(yán)格管理的,這種商業(yè)性的行為是違法的。”
即使是在專業(yè)期刊進(jìn)行宣傳,藥品以“安全性”“功效”來作為賣點(diǎn)和優(yōu)勢也是法律不允許的。《廣告法》規(guī)定,醫(yī)療、藥品、醫(yī)療器械廣告不得含有表示功效、安全性的斷言或者保證。國家市場監(jiān)管總局也有規(guī)定:藥品相關(guān)廣告不得包含“安全”“安全無毒副作用”“毒副作用小”等內(nèi)容。
但監(jiān)管滯后使得違規(guī)營銷行為屢禁不止,其根源在于企業(yè)對流量的盲目追逐。部分藥企在產(chǎn)品獲批后,為拓展市場默許甚至縱容第三方做“素人分享”“博主種草”類推廣,卻對處方藥營銷的合規(guī)底線置之不理。
最終,違規(guī)用藥不僅會危害個人健康,還可能引發(fā)耐藥性等公共衛(wèi)生問題。
03
流感藥物不需要“神”
告別“神藥”崇拜,理性看待抗流感藥的實(shí)際價值才是正解。
新一代流感藥的風(fēng)險尚未被充分認(rèn)知,與之形成鮮明對比的,是奧司他韋的“常青樹”地位,該藥是迄今為止使用最廣泛的治療及預(yù)防流感的抗病毒藥物,可適用于孕婦、哺乳期女性、5歲以下兒童等高危人群。
對行業(yè)來說,只有摒棄對“神藥”的網(wǎng)紅式營銷心態(tài),通過長周期臨床觀測積累數(shù)據(jù),不斷將研究覆蓋至更廣泛的人群,逐步填補(bǔ)不良反應(yīng)的認(rèn)知空白,才能完善藥品說明書,讓藥物在合規(guī)前提下被民眾安全使用。
只有將“安全”從宣傳口號轉(zhuǎn)化為業(yè)內(nèi)共識與行動準(zhǔn)則,中國抗流感用藥才能走出“一代版本一代神”的認(rèn)知誤區(qū),真正研發(fā)出下一代可長期應(yīng)用的抗流感藥物。




